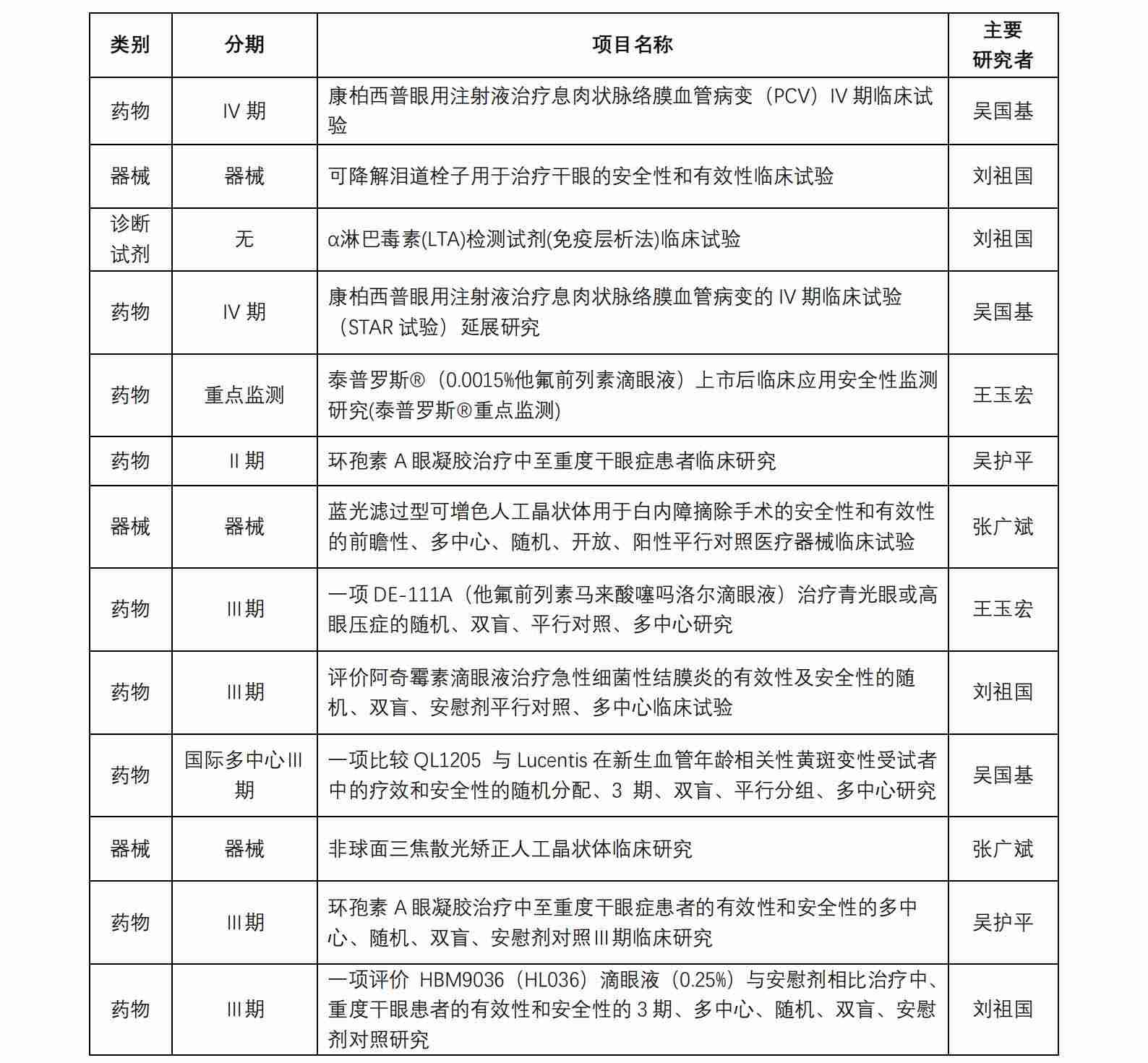
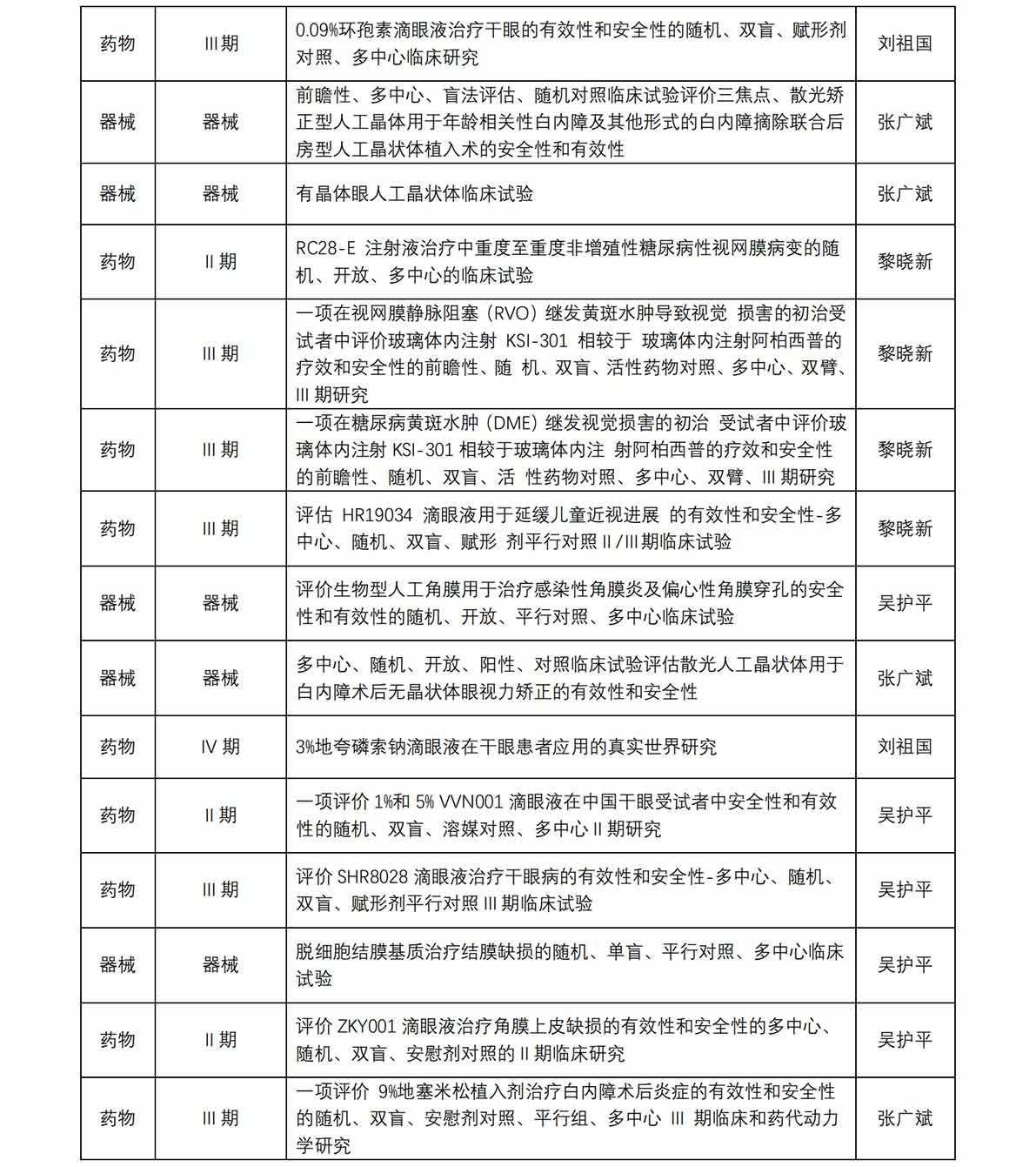
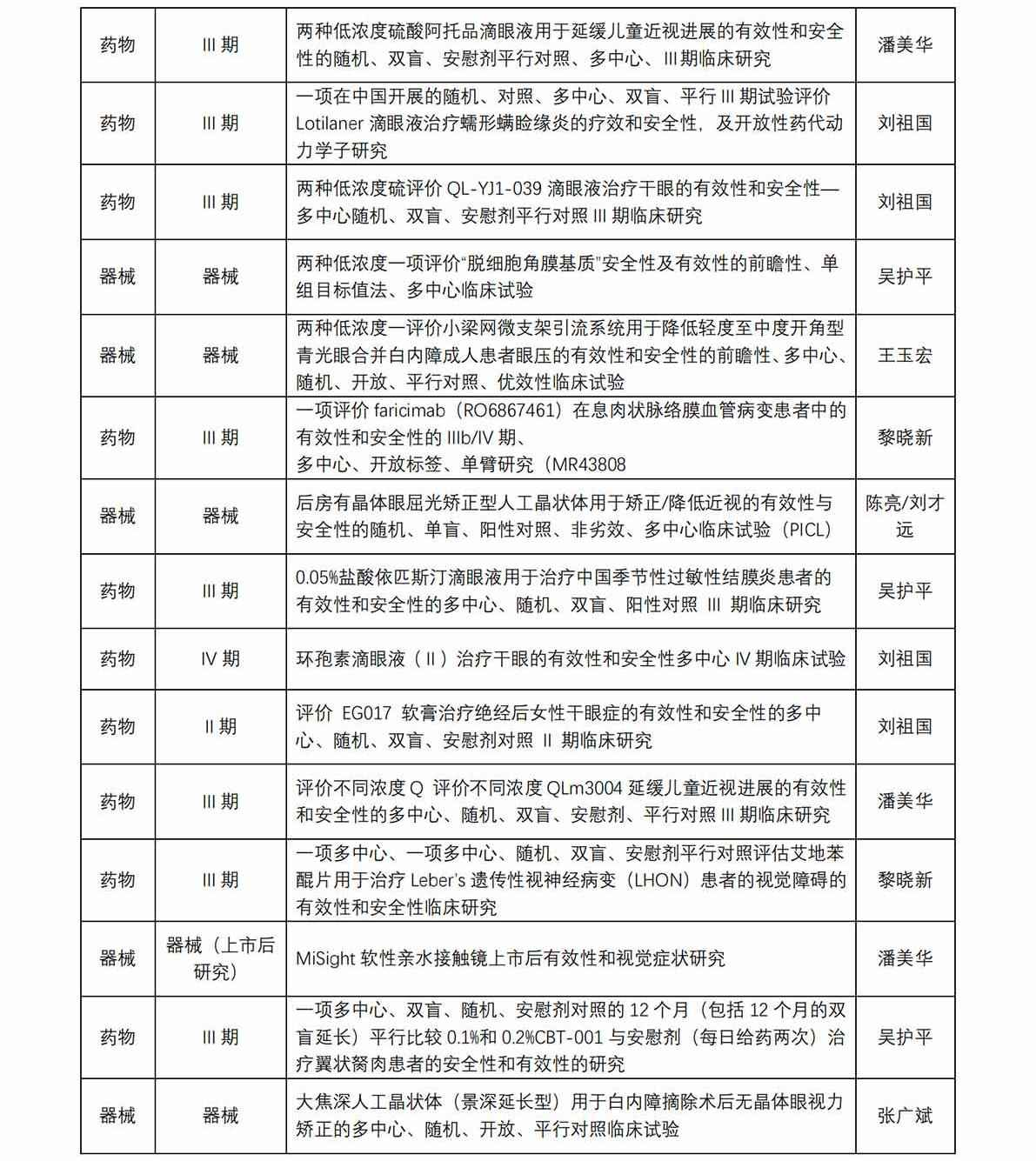
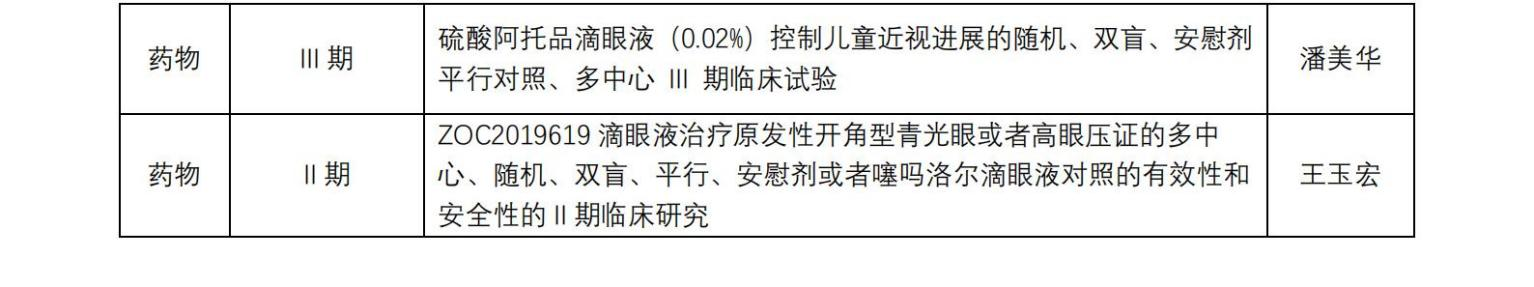
福建省已启动重大突发公共卫生事件一级响应,为做好疫情防控, 保障受试者以及相关临床研究人员的健康安全,近期对我院临床试验相关工作进行如下调...[详细]
关于印发药物临床试验伦理审查工作指导原则的通知 国食药监注[2010]436号 2010年11月02日 发布 各省、自治区、直辖市食品药品监督管理局(药品监督管理局...[详细]
为了科学、规范地开展临床药物试验,提高我院临床和科研整体水平,确保药物临床试验的科学性和可靠性,以及受试者的权益、安全和健康……...[详细]
厦门大学附属厦门眼科中心药物临床试验伦理委员会名单...[详细]
厦门大学附属厦门眼科中心药物临床试验机构成员名单...[详细]
因人事变动和药物临床试验工作实际需要,经研究决定,对药物临床试验伦理委员会名单进行调整……...[详细]
为细化临床试验项目的申报、启动等各项工作,确保项目开展符合法规要求,保证项目质量,现提供《项目启动SOP》、《遗传办申报SOP》等指南文件,供各...[详细]
人类遗传资源管理条例 (送审稿) 第*章 总 则 第*条 为了规范和促进我国人类遗传资源的保护和利用,增强我国生物和医药科技的研究开发能力,保障人...[详细]
...[详细]
世界医学协会赫尔辛基宣言 人体医学研究的伦理准则 赫尔辛基宣言在第18届世界医学协会联合大会(赫尔辛基,芬兰,1964年6月)采用,并在下列联合大会...[详细]
《涉及人的生物医学研究伦理审查办法》已于2016年9月30日经国家卫生计生委委主任会议讨论通过,现予公布,自2016年12月1日起施行……...[详细]
第一章 总 则 第一条 为保证药物临床试验过程规范,数据和结果的科学、真实、可靠,保护受试者的权益和安全,根据《中华人民共和国药品管理法》《中...[详细]
医疗器械临床试验质量管理规范 第一章 总 则 第一条 为加强对医疗器械临床试验的管理,维护受试者权益和安全,保证医疗器械临床试验过程规范,结果...[详细]
伦理审查申请 / 报告指南 为指导主要研究者/申办者、课题负责人提交药物/器械/诊断试剂临床试验的伦理审查申请/报告,特制定本指南。 第一章 提交伦理...[详细]
伦理审查流程 1.申请人提交送审项目材料。 一般由主要研究者负责送审材料。药物、器械的申办者一般负责准备送审材料。多中心试验的年度/跟踪审查报...[详细]
伦理委员会章程 第一章 总 则 第一条 为保护临床研究受试者的权益和安全,规范本伦理委员会的组织和运作,根据国家食品药品监督管理局《药物临床试...[详细]
正常值范围...[详细]
为方便各位同仁开展临床试验项目相关工作,特整理有关日常目录表单模板如下,请各申办方根据需求下载使用。洽谈项目请联系机构办公室:0592-2367670。...[详细]
请各位CRA按项目需要下载各年度室间质控证书及仪器检定报告。...[详细]
本中心伦理委员会所需要递交的文件详见附件。...[详细]


扫描二维码关注厦门大学附属厦门眼科中心微信

扫描二维码入群获取更多眼科资讯